几种蛋白质提取方法的原理有什么?
写在前面······
Western Blot蛋白样品制备是实验的第一步,也是非常关键的一步,只有蛋白提得质量好,后面Western Blot跑出来的条带结果才美观又可靠。不同的样本,提取蛋白的方法不同,像诸如血浆、消化液和分泌液等体液中可溶性蛋白质,可不经抽提直接进行分离。而胞内蛋白的抽提则需要先将细胞膜或细胞壁破碎,然后用适当溶剂将蛋白质溶出,再用离心法除去不溶物,得到抽提液。
这一篇推文我们先对蛋白抽提的整体步骤和手段做一介绍,下面这张图系统地概括了严格意义上蛋白抽提的步骤,实际上对于我们大部分同学来说,只做到红框里的内容就足以满足实验需求了:
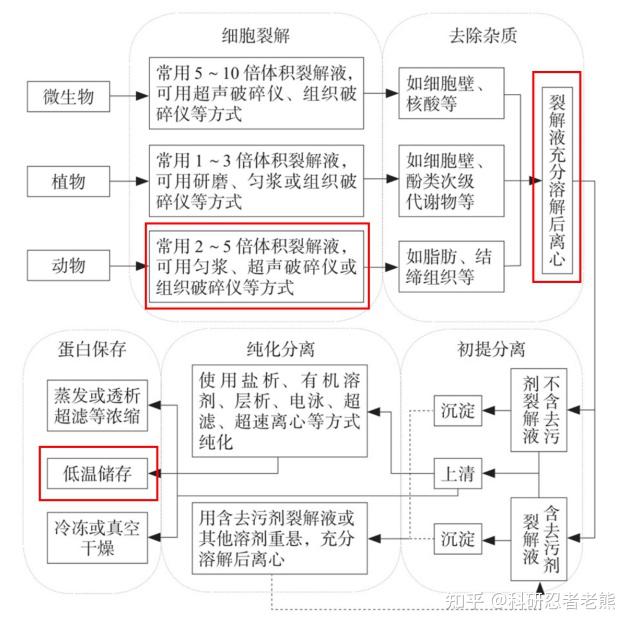
下面我们来介绍一下总体步骤:
一、分离组织/细胞
组织/细胞分离需要主要依据实验目的选择所需的实验材料:
1、培养的悬浮细胞或细菌菌液,或者血液、尿液、胸腔积液等体液可直接离心收集待用;
2、贴壁培养的细胞用PBS清洗后收集待用;
3、动物组织或手术标本,必须新鲜处理,取得实验所需的脏器或组织,剔除结缔组织及脂肪组织后用预冷的生理盐水或PBS洗去血液或其他体液(如心脏、大脑、肝脏等必要时可以用灌注法洗去脏器内部血液),再用滤纸吸去多余水分后收集待用。如不能立即进行实验,需要冻到-80℃。
二、组织/细胞破碎裂解
除了分泌型细胞外蛋白可以直接离心使用外,更多时候我们需要先将组织/细胞破碎,使蛋白充分释放到溶液中,才能进行后续提蛋白操作。不同生物体或同一生物体的不同组织,其细胞破坏难易不一,使用方法也不完全相同。如动物胰腺、肝脏、脑组织一般较柔软,作普通匀浆器研磨即可;肌肉及心脏组织较韧,需预先绞碎再制成匀浆。常用组织细胞的破碎方法如下:
(一)研磨或匀浆
适用于组织材料,取适量组织剪碎后加入适当的生理盐水或PBS等缓冲液后进行研磨或匀浆:
1.研钵研磨
将研钵置于冰上预冷,将组织及缓冲液放入后用力研磨成稠糊状,也可加氧化铝、石英砂及玻璃粉磨细(在磨细时局部往往生热导致变性或pH显著变化,尤其用玻璃粉和氧化铝时,另外磨细剂的吸附也可导致蛋白质的损失),离心后取上清液。
2.手持式电动匀浆器
多数为硬质塑料材质,靠钻头与EP管内壁两个面摩擦将组织磨碎。由于两面间隔只有几十至几百微米,对细胞破碎程度比高速捣碎机高,机械切力对分子破坏较小。
3.高通量组织破碎仪
加入适量的金属或玻璃等不同材质的珠子,靠机器高速敲击管壁震动从而使得组织破碎。
(二)超声波处理法
用一定功率的超声波处理细胞悬液,使细胞急剧震荡破裂,此法多适用于微生物材料。超声的频率和功率根据实验目的不同而改变,超声时需要分为几个周期,比如超声几秒,停几秒,一共超声多少次,一般超声5-10s,反复多次。超声的优点在于耗时短,肽链提取片段长度更可控,回收率更高。缺点是在处理过程较难避免溶液中出现气泡,并容易大量产热,需要让容器置于冰上,过强的超声波可导致多聚物降解和蛋白失活。如果超声出现沉淀说明超声功率太大。
(三)反复冻融法
在冰箱冷藏或干冰中-20~-15℃冻固后,再缓慢地融解,如此反复操作,使大部分细胞及细胞内颗粒破坏。由于渗透压的变化,使结合水冻结产生组织变性,冰晶碎片将细胞膜刺碎,使蛋白质可溶化,成为黏稠的浓溶液,但脂蛋白冻结变性。这个方法成本低,操作简便,单过程缓慢,不适用于对温度比较敏感的蛋白质。
(四)酶法
使用分解细胞壁或细胞膜成分的酶类使得细胞破裂。如溶菌酶能专一性地破坏细菌细胞壁;水解糖肽组分的β-1,4-糖苷键,使细胞内含物释放出来,特别适用于革兰氏阳性细菌。
(五)有机溶剂法
粉碎后的新鲜材料在0℃以下加入5~10倍量的丙酮,迅速搅拌均匀,可破碎细胞膜,破坏蛋白质与脂质的结合。蛋白质一般不变性,脱脂和脱水后变为干燥粉末。用少量乙醚洗涤,经滤纸干燥后,如脱氢酶等可保存数月不失去活性。
(六)表面活性剂法
这个是我们实验中相对用得比较多的方法。常用的溶剂的有十二烷基磺酸钠(SDS)、氯化十二烷基吡啶及去氧胆酸钠等,非离子型表面活性剂吐温40(Tween 40)或Triton X-100等,这些溶剂能破坏细胞膜使细胞瓦解,有时使蛋白质更易溶解,除去表面活性剂后蛋白质仍留在上清液中。
以上方法普遍适用大多数样本,无论用哪一种方法破碎组织细胞,都会使细胞内蛋白质或核酸水解酶释放到溶液中,使大分子降解,导致天然物质量的减少。加入二异丙基氟磷酸(DFP)可以抑制或减慢自溶作用;加入碘乙酸可以抑制活性中心需要有巯基的蛋白水解酶的活性;加入苯甲磺酰氟化物(PMSF)也能清除蛋白水解酶活力;还可通过调整pH、温度或离子强度等,使之适合于目的蛋白质的提取。
三、提取目的蛋白
蛋白质提取的基本原理不外乎两方面:一是利用混合物中几个组分分配率的差别,把它们分配到可用机械方法分离的几个物相中,如盐析、有机溶剂提取、层析和结晶等;二是将混合物置于单一物相中,通过物理力场的作用使各组分分配于相同区域而达到分离目的,如电泳、超速离心、超滤等。
大部分蛋白质都可溶于水、稀盐、稀酸或碱溶液,少数与脂类结合的蛋白质则溶于乙醇、丙酮、丁醇等有机溶剂中。因此,可采用不同溶剂提取分离和纯化蛋白质。
(一)水溶液提取法
抽提蛋白质的理想条件是尽可能促进蛋白质在溶剂中溶解,而减弱蛋白水解酶的活力,以减少细胞的自溶过程。主要通过选择适当pH,温度或溶剂,以及加适当蛋白水解酶抑制剂。
稀盐缓冲系统的水溶液对蛋白质稳定性好、溶解度大,是提取蛋白质最常用的溶剂,通常用量是原材料体积的1~5倍,提取时需要均匀地搅拌,以利于蛋白质的溶解,提取的温度要视有效成分性质而定。一方面,多数蛋白质的溶解度随着温度的升高而增大,因此温度高利于溶解,缩短提取时间。另一方面,温度升高会使蛋白质变性失活,因此基于这一点考虑提取蛋白质时一般采用低温(4℃以下)操作。为了避免蛋白质在提取过程中降解,可加入蛋白水解酶抑制剂(如二异丙基氟磷酸、碘乙酸等)。下面着重讨论提取液的pH和盐浓度的选择。
1.pH
蛋白质是具有等电点的两性电解质,提取液的pH应选择在偏离等电点两侧的pH范围内。用稀酸或稀碱提取时,应防止过酸或过碱而引起蛋白质可解离基团发生变化,从而导致蛋白质构象的不可逆变化。一般来说,碱性蛋白质用偏酸性的提取液提取,而酸性蛋白质用偏碱性的提取液。
2.盐浓度
稀浓度可促进蛋白质的溶解,称为盐溶作用。同时稀盐溶液因盐离子与蛋白质部分结合,具有保护蛋白质不易变性的优点,因此在提取液中加入少量NaCl等中性盐,一般以0.15mol/L浓度为宜,这也是为什么我们在做免疫共沉淀时的RIPA裂解液里含有150 mM NaCl。缓冲液常采用0.02~0.05mol/L磷酸盐和碳酸盐的等渗盐溶液。
(二)有机溶剂提取法
一些和脂质结合比较牢固或分子中非极性侧链较多的蛋白质,不溶于水、稀盐溶液、稀酸或稀碱,可用乙醇、丙酮和丁醇等有机溶剂。它们具有一定的亲水性,还有较强的亲脂性,是理想的脂蛋白提取液,但必须在低温下操作。丁醇提取法对提取一些与脂质结合紧密的蛋白质特别优越,一是因为丁醇亲脂性强,特别是溶解磷脂的能力强;二是丁醇兼具亲水性,在溶解度范围内不会引起蛋白质的变性失活。另外,丁醇提取法的pH及温度选择范围较广,也适用于动植物及微生物材料。
好了,今天就总结到这里,总的来说蛋白样品制备决定成败的关键一步,后面我会详细总结抽提细胞蛋白的步骤和一些避雷操作,别忘了点赞、转发、关注,让我有动力继续分享!
参考文献
[1] J.萨姆布鲁克, D.W.拉塞尔. 分子克隆实验指南[M]. 科学出版社, 2002.
[2] 林秋雄, 吴炳义. 生物医学基础研究使用手册[M]. 人民卫生出版社, 2021
[3] 陶永光. 肿瘤分子生物学与细胞生物学实验手册[M]. 湖南科学技术出版社, 2014.
往期精彩:
呕心沥血总结:为什么你的Western blot图总是跑得那么丑?
一文掌握重组蛋白如何选择表达系统
实验知多少之一文掌握流式细胞术检测原理
Western blot 实验进阶版之磷酸化蛋白检测那点事儿